日本初の遺伝子治療薬は世界に羽ばたくのか、アンジェス山田社長に聞く
株探プレミアム・リポート
ビジネス誌、マネー誌などをへて、2018年4月にみんかぶ(現ミンカブ・ジ・インフォノイド)に入社。現在に至る。
日本初の遺伝子治療薬は世界にいつ羽ばたくのか。バイオ創薬企業のアンジェス <4563> が開発した日本初の遺伝子治療薬「コラテジェン」が9月に薬価収載され、販売を開始した(販売元は田辺三菱製薬 <4508> )。
創業から20年をかけて悲願の発売に至ったものの、足元のアンジェス株は冴えない。8月末に直前高値の965円から560円に半値近くに下落し、その後もみ合いながら、株価が乱高下する状況に。8月末に明かされた同薬の薬価が約60万円と、投資家の期待に届かなかったことが要因と見られている。
株価には落胆の声が色濃く反映されている中で、エース経済研究所の池野智彦シニアアナリストは「コラテジェンはそもそも国内販売だけでアンジェスの業績を黒字転換する力はないことは想定されていたこと。むしろ国内販売の開始で、米国での治験開始、そして製造承認の獲得に一歩近づいた点では、前向きに捉えられる」という。
日本初の遺伝子治療薬は国内から米国、そして世界各国へと広がりをみせるのか。アンジェスの山田英社長に聞いた。
■アンジェスが開発した日本初の遺伝子治療薬「コラテジェン」
――足の血管が詰まり重症な症状を持つ患者に投与する「コラテジェン」が9月4日から販売(薬価収載)されました。開発途上では2008年3月に一度、承認申請しましたが10年9月に取り下げ後、再チャレンジしての販売。これまでを振り返ると、感慨もひとしおというところでしょうか
山田英社長(以下:山田): もちろんうれしいのですが、今回の承認は仮承認(条件付き早期承認制度による承認)の段階です。これからさらにデータを積み上げて、本承認を取得する努力をしていかなくてはなりません。
――仮承認後の投与と、治験段階での投与とで、何か違いはあるのでしょうか。
山田 特段の違いはありません。
60万円の薬価、ピーク時売上高12億円、投与患者数992人の想定
――今年8月28日の中央社会保険医療協議会(中医協)の総会で了承された保険償還価格は、「60万360円」(4mg1.6mL 1瓶あたり)となりました。想定より低く抑えられたという評価が多いようですが。
山田 その点について我々から申し上げられるのは、今回の価格は当局と合意したものであり、我々は決まった条件で粛々とやるべきことをやる、ということに尽きます。
薬価に関して付け加えるとすれば、今回の承認では1人の患者さんに投与するのは通常2回、場合によっては3回まで認められていることです。つまりは患者さん1人に対して薬価の2倍ないしは3倍の販売額になることです。
■中医協総会で示されたコラテジェンの保険償還価格の資料

――今年5月14日に販売開始の延期をアナウンスされました。これは当初、決まっていた薬価の見直し交渉をするためだと解説する向きもありますが。
山田 そうした見方が医療関係者や市場関係者の間にあるようですが、我々からコメントすべきことは特にありません。
――ピーク時の患者数が992人というのも、従前の想定よりかなり少なくなったという印象があります。中医協の資料では、使用目的として、「標準的な薬物治療の効果が不十分で、血行再建術の施行が困難な慢性動脈閉塞症における潰瘍の改善」とあります。つまり、当初の想定より投与する患者が絞られたことがその要因でしょうか。
山田 繰り返しですが、これも当局と合意した数字ですので、我々はそれに則って、進めていくことにつきます。適用する症状については、我々は当初、HGF遺伝子治療薬(コラテジェン)の投与で、「潰瘍」の改善と「疼痛」の改善という2つで承認を目指しました。
質問にありますように今回の承認では「潰瘍」の改善のみとなりました。我々は引き続き疼痛の改善での承認を目指して、開発を進めていきます。仮にそれが実現すれば、今回決まったのは異なる条件や予測が加わることもあり得えます。
――対象となる国内患者は、年間に5000~1万5000人という見方もありましたが。
山田 これについても、我々から申し上げられることは特にありません。
■アンジェスの日足チャート
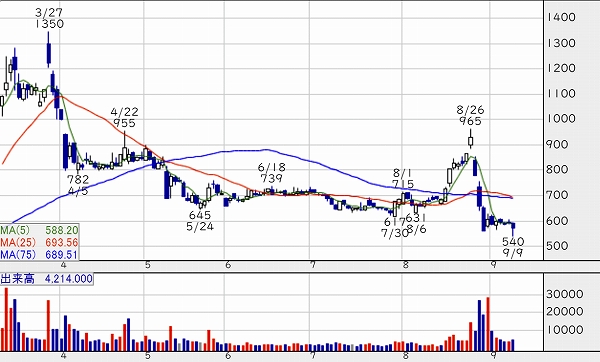
※当該情報は、一般情報の提供を目的としたものであり、有価証券その他の金融商品に関する助言または推奨を行うものではありません。
